À propos de ce livret
Le Complexe I est la première et la plus grande enzyme de la chaîne respiratoire mitochondriale, où l’énergie libre des électrons est convertie en translocation de protons à travers la membrane interne mitochondriale (IMM).
L’énergie qui déplace un proton à travers la membrane n’est pas une énergie chimique au sens de l’ATP, mais une énergie libre électronique, extraite du NADH lors du flux d’électrons le long du gradient redox.
La force motrice globale correspond à la différence de potentiel standard entre le couple NADH/NAD⁺ (≈ −320 mV) et O₂/H₂O (+820 mV), soit ΔG°’ ≈ −220 kJ·mol⁻¹ par 2 électrons.
Le Complexe I réalise la première étape de conversion de cette énergie en force proton-motrice (Δp), en capturant une partie de cette énergie libre tandis que le reste est dissipé sous forme de chaleur et d’entropie.
Ce eBook éducatif (avril 2026) est conçu pour les étudiants de doctorat et de médecine et fournit un cadre rigoureux reliant transfert d’électrons, mécanismes moléculaires et thermodynamique au pompage de protons.
Structure du livret
Ce PDF de 10 pages est structuré comme un cours compact :
- Page de couverture
- Préface
- Table des matières
- 2 chapitres principaux
- 2 annexes (équations et glossaire)
Concepts fondamentaux développés dans le livret
L’énergie libre des électrons comme force motrice
- ΔG°’ = −nFΔE°’ comme relation fondamentale
- NADH → O₂ libère ~−220 kJ·mol⁻¹
- Le Complexe I capture la première étape d’environ ~−70 kJ·mol⁻¹
- Le pompage de protons est un travail thermodynamiquement « ascendant » (contre le gradient)
Mécanisme moléculaire — un piston piloté par les réactions redox
- Structure en L (~1 MDa, 45 sous-unités)
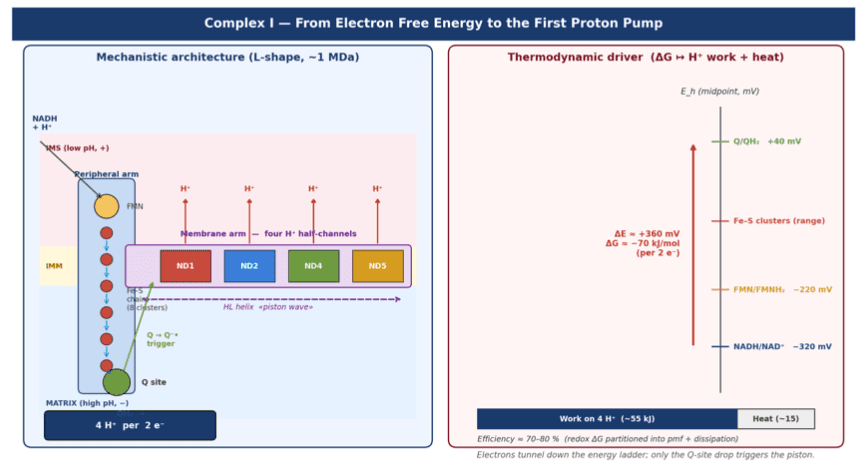
- Bras redox : FMN + clusters Fe–S (N1a → N2)
- Bras membranaire : canaux à protons dans ND1, ND2, ND4, ND5
- Le semiquinone (Q⁻•) agit comme déclencheur mécanique
- Hélice HL : transducteur conformationnel longue distance (~60 Å)
Voie de transfert électronique :
NADH → FMN → Fe–S clusters → Q → QH₂
Le transfert d’électrons ne lie pas directement les protons : il déclenche une onde conformationnelle qui active leur translocation via des canaux à accès alterné.
Stœchiométrie et comportement du système
- 1 NADH → 2 e⁻ → 4 H⁺ pompés par le Complexe I
- Rendement total de la chaîne respiratoire : 10 H⁺ par NADH
- Transport inverse d’électrons (RET) en condition de Δp élevé
- Source majeure de ROS en état hyperpolarisé
- Transition A↔D régulant l’activité en ischémie
Cadre quantitatif et thermodynamique
- ΔE (NADH → Q) ≈ +0.36 V
- ΔG ≈ −70 kJ·mol⁻¹
- Δp ≈ 180–220 mV
- Travail requis : ~+77 kJ·mol⁻¹ pour 4 H⁺
- Rendement ≈ 70–80 %
Relations clés :
- ΔG°’ = −nFΔE°’
- Δp = ΔΨ_m − (2.303 RT/F)·ΔpH
Le Complexe I fonctionne près de l’équilibre thermodynamique, mais dissipe volontairement une partie de l’énergie afin de maintenir un flux unidirectionnel — expression directe de la deuxième loi de la thermodynamique.
Pertinence clinique et translationnelle
- Déficits du Complexe I (Leigh, MELAS, LHON)
- Lésions d’ischémie-reperfusion et ROS via RET
- Metformine comme inhibiteur réversible du Complexe I
- Pathologies d’hyperpolarisation vs dépolarisation
- Rôle central dans la dysfonction mitochondriale et la défaillance énergétique
Repères clés d’apprentissage
- « Le premier proton est payé par ~70 kJ·mol⁻¹ d’énergie libre électronique »
- Le semiquinone (Q⁻•) est un déclencheur mécanique, pas un réservoir énergétique
- L’hélice HL est un transducteur mécanique longue distance
- Rendement < 100 % = production nécessaire d’entropie
À qui s’adresse ce contenu ?
- Doctorants en bioénergétique et biologie moléculaire
- Médecins intéressés par la physiologie mitochondriale
- Chercheurs en biologie redox
- Cliniciens explorant les dysfonctionnements mitochondriaux
Aperçu clé
Le Complexe I est un moteur mécanique piloté par les réactions redox, qui convertit l’énergie libre des électrons en pompage de protons, initiant ainsi la force proton-motrice et la production d’énergie cellulaire.
Note : Le PDF complet est en anglais.