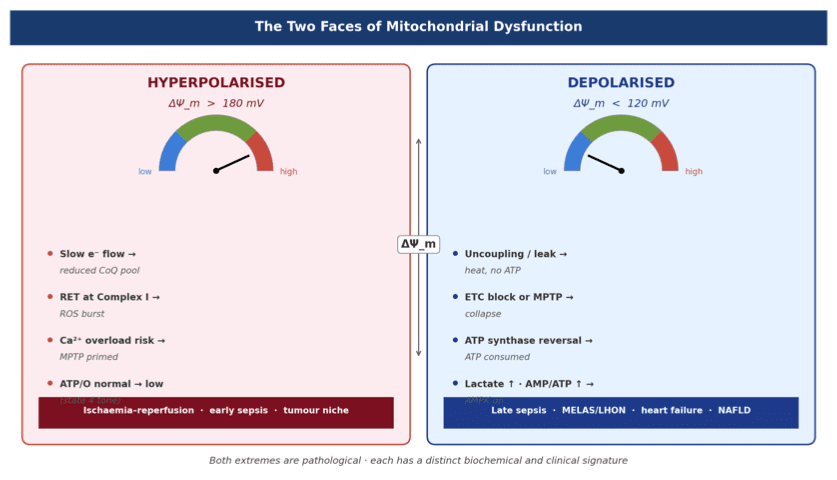
Le principe biologique fondamental
Chaque macrophage effectue un choix thermodynamique. Il peut fonctionner par phosphorylation oxydative (OXPHOS) – un métabolisme à haute efficacité et faible entropie – ou basculer vers la glycolyse aérobie – un mode rapide, énergivore et à haute entropie. Cet axe thermodynamique détermine si la cellule immunitaire guérit ou nuit à l’hôte.
Ce compromis bioénergétique n’est pas une conséquence secondaire de la maladie. C’est le moteur moléculaire de la maladie. La même logique s’applique de manière identique à trois pathologies cliniquement distinctes : la septicémie, la polyarthrite rhumatoïde et le cancer du poumon.
Comparaison des phénotypes bioénergétiques
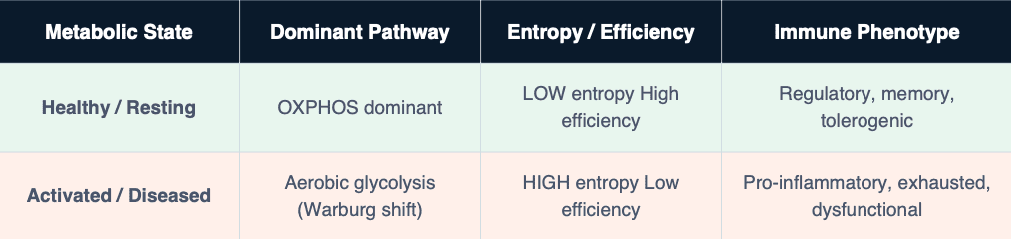
1. Septicémie — Quand le moteur surchauffe
Dans la septicémie, les signaux bactériens provoquent l’effondrement du potentiel de membrane mitochondriale (∆Ψm), inondent la cellule d’espèces réactives de l’oxygène (ROS) et forcent un basculement métabolique de l’OXPHOS vers la glycolyse. Il en résulte une hyperpolarisation des macrophages M1 : libération massive de IL-1β, TNF-α et IL-6 — la tempête cytokinique. Ce n’est pas simplement de l’inflammation ; c’est une défaillance thermodynamique. La cellule dissipe l’énergie sous forme de chaleur et d’entropie au lieu de produire un travail biologique utile.
Mécanismes moléculaires
• Explosion de ROS (Complexes I/III) → stabilisation de HIF-1α → activation des gènes glycolytiques
• Perte du ∆Ψm → défaut de couplage de l’ATP synthase → fuite de protons sous forme de chaleur
• Libération de mtDNA → activation cGAS-STING → amplification de la réponse innée
• Accumulation de succinate → stabilisation de HIF-1α et IL-1β
✓ Traduction clinique
• Précurseurs de NAD+ (NMN, NR) : restaurent la disponibilité des cofacteurs du complexe I, rétablissent la capacité OXPHOS et réduisent la production de cytokines M1 dans les modèles précliniques de septicémie.
• Antioxydants ciblant les mitochondries (MitoQ, SS-31) : éliminent le superoxyde généré dans la membrane mitochondriale interne (IMM), préservent le ∆Ψm et atténuent les lésions organiques dans les modèles CLP.
• Opportunité de biomarqueur : ratio OCR/ECAR (consommation d’oxygène vs acidification extracellulaire) comme indice métabolique au lit du patient de l’état inflammatoire des macrophages.
2. Polyarthrite rhumatoïde — L’entropie comme état chronique
L’articulation synoviale dans la polyarthrite rhumatoïde est un microenvironnement à entropie élevée permanente : hypoxique, appauvri en glucose, acide et saturé de lactate. Les lymphocytes T CD4+, les macrophages et les synoviocytes de type fibroblastique convergent vers la glycolyse aérobie pour survivre. Ce basculement métabolique est l’inflammation elle-même : il maintient HIF-1α, alimente NF-κB et active en continu l’inflammasome NLRP3. Pendant ce temps, les cellules T régulatrices (Treg), qui dépendent de l’oxydation des acides gras et de l’OXPHOS pour leur fonction suppressive, sont métaboliquement privées de substrats dans ce même environnement.
Mécanismes moléculaires
• HIF-1α → augmentation de GLUT1/LDHA → augmentation du flux glycolytique → production de IL-17 et IL-6
• ROS mitochondriaux → activation de NF-κB et NLRP3 → boucle cytokinique persistante
• Activation de mTORC1 → suppression de l’OXPHOS → orientation des cellules T de Treg vers Th17
• Treg dépendantes de l’oxydation des acides gras (FAO) : privation de substrats thermodynamiques (faible disponibilité lipidique en milieu hypoxique) = perte de régulation immunitaire
✓ Traduction clinique
• Metformine : inhibiteur du complexe I → active AMPK, restaure l’équilibre métabolique et réduit le flux glycolytique dans les cellules immunitaires de la PR. Effet anti-inflammatoire indépendant de son action hypoglycémiante.
• Inhibiteurs de mTOR (analogues de la rapamycine) : réorientent les cellules T de Th17 vers Treg en levant la répression de l’OXPHOS et de la FAO.
• Opportunité de biomarqueur : ratio P/O (ATP produit par O₂ consommé) et ratio NAD+/NADH dans les cellules immunitaires synoviales comme indicateurs quantitatifs de l’activité de la maladie.
3. Cancer du poumon — La tumeur comme piège thermodynamique
Les tumeurs pulmonaires exportent de l’entropie dans leur microenvironnement. Elles consomment le glucose de manière intensive via l’effet Warburg, libèrent du lactate qui acidifie le milieu et épuisent l’oxygène — créant une prison thermodynamique pour les lymphocytes infiltrant la tumeur (TILs). Ces derniers présentent une diminution de la consommation d’oxygène, une réduction de la masse mitochondriale et un effondrement du ∆Ψm. L’épuisement des cellules T n’est pas seulement un programme transcriptionnel — c’est un effondrement bioénergétique. La tumeur ne se contente pas d’échapper au système immunitaire : elle le prive de ressources.
Mécanismes moléculaires
• Glycolyse de type Warburg dans les cellules tumorales → efflux de lactate → acidification du microenvironnement tumoral (TME) → inhibition de l’OXPHOS des cellules T
• Déplétion en glucose/glutamine dans le TME → TILs privés de substrats → perte de ∆G effectif
• Hypoxie → activation de HIF-1α dans la tumeur → augmentation de VEGF/PD-L1 → exclusion immunitaire et épuisement des checkpoints
• Phénotype TIL CD36 élevé : excès d’absorption lipidique → surcharge mitochondriale en lipides → sensibilité accrue à la ferroptose
✓ Traduction clinique
• Combinaison métabolique + immunothérapie : les activateurs de l’OXPHOS (urolithine A, NMN) associés aux anti-PD-1 montrent une réactivation synergique des TILs dans les modèles précliniques de NSCLC.
• Intervention nutritionnelle : la restriction en méthionine réduit la suppression des Treg ; la supplémentation en glutamine restaure la capacité respiratoire des TILs.
• Opportunité de biomarqueur : profilage OCR des TILs (technologie Seahorse) avant traitement ; IRM au pyruvate 13C hyperpolarisé pour une cartographie métabolique en temps réel du microenvironnement tumoral.
Perspective thermodynamique et quantitative
Chaque maladie représente une déviation mesurable de l’efficacité thermodynamique. Les variables clés ne sont pas uniquement moléculaires — ce sont des paramètres bioénergétiques quantifiables pouvant être suivis en clinique :
• ∆Ψm (potentiel de membrane mitochondriale) : indicateur de la force proton-motrice et du couplage de l’OXPHOS. Son effondrement précède la dysfonction immunitaire.
• Ratio P/O (efficacité de phosphorylation) : quantité d’ATP produite par molécule d’O₂ consommée. Diminue lors de la reprogrammation inflammatoire.
• Ratio OCR/ECAR : consommation d’oxygène vs taux d’acidification extracellulaire — indice en temps réel de l’équilibre OXPHOS/glycolyse.
• Ratio NAD+/NADH : capteur redox central. Un NAD+ faible = OXPHOS altéré, entropie élevée, régulation immunitaire dépendante des sirtuines compromise.
• Nombre de copies de mtDNA / mtDNA cytosolique : indicateur de l’accumulation d’entropie mitochondriale et de l’activation innée médiée par les DAMPs.
Vers un cadre clinique unifié
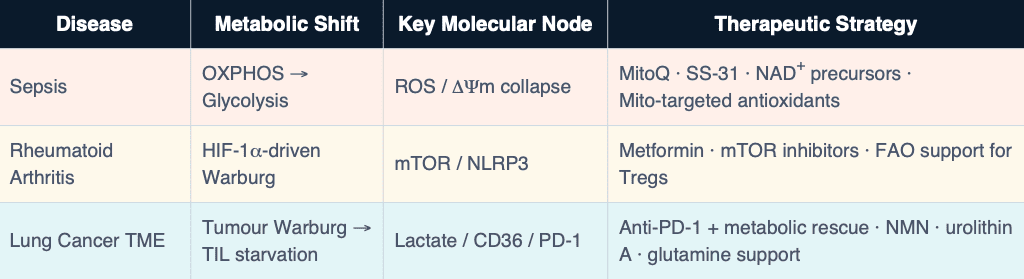
Vers quoi cela évolue : les biomarqueurs immunitaires de nouvelle génération
La prochaine génération de biomarqueurs immunitaires ne se limitera pas aux cytokines. Elle sera métabolique :
• Ratio OCR/ECAR dans les cellules immunitaires du sang périphérique
• Potentiel de membrane mitochondriale (∆Ψm) comme indice d’activation immunitaire
• Ratio NAD+/NADH comme score systémique de santé bioénergétique
• Taux de libération du mtDNA comme marqueur en temps réel de production d’entropie
• Ratio lactate/pyruvate urinaire comme indicateur non invasif du basculement glycolytique
Les thérapies à venir ne se contenteront pas de bloquer des récepteurs — elles restaureront l’ordre thermodynamique dans les cellules immunitaires qui l’ont perdu. C’est la promesse de l’immunométabolisme : non pas davantage d’immunosuppresseurs, mais des stratégies bioénergétiques plus intelligentes qui redonnent aux cellules immunitaires ce que la maladie leur a retiré.
La réponse pourrait se trouver dans les mitochondries.
Base de preuves sélectionnées
1. Ji F et al. Crosstalk of mitochondrial dysfunction and macrophage polarization in sepsis. Front Immunol. 2026.
2. Xie R et al. Roles of immune cell metabolism in rheumatoid arthritis. Front Immunol. 2026.
3. Eivazzadeh Y et al. Immunometabolism in lung cancer. iScience. 2026.
4. Dwivedi V et al. Mitochondrial dysfunction and cellular senescence in ageing sarcopenia. Mol Biol Rep. 2026.
5. Seledtsov V. Mitochondria-targeted therapy in anti-aging medicine. J Biol Methods. 2026.
6. Glogowski PA et al. Reprogramming the mitochondrion in atherosclerosis. Antioxidants. 2025.
7. Xu Y et al. Nutritional intervention alleviates T cell exhaustion and empowers anti-tumor immunity. Front Immunol. 2026.
8. Zhang XY et al. The role of CD36 in immune function. Front Immunol. 2026.
Ce document est une communication scientifique fondée sur des données probantes, destinée aux professionnels de santé, aux chercheurs et aux étudiants avancés. Toutes les affirmations reposent sur la littérature évaluée par les pairs à jour au premier trimestre 2026. Il ne constitue pas une recommandation clinique directe.