Sobre este cuaderno
El Complejo I es la primera y mayor enzima de la cadena respiratoria mitocondrial, donde la energía libre de los electrones se convierte en translocación de protones a través de la membrana interna mitocondrial (IMM).
La energía que mueve un protón a través de la membrana no es energía química en el sentido del ATP, sino energía libre electrónica, obtenida del NADH a medida que los electrones descienden por un gradiente redox.
La fuerza impulsora global corresponde a la diferencia de potencial entre el par NADH/NAD⁺ (≈ −320 mV) y O₂/H₂O (+820 mV), es decir ΔG°’ ≈ −220 kJ·mol⁻¹ por 2 electrones.
El Complejo I realiza la primera etapa de conversión de esta energía en fuerza protón-motriz (Δp), capturando parte de la energía libre mientras el resto se disipa como calor y producción de entropía.
Este eBook educativo (abril de 2026) está diseñado para estudiantes de doctorado y medicina y proporciona un marco riguroso que conecta transferencia de electrones, mecanismos moleculares y termodinámica con el bombeo de protones.
Estructura del cuaderno
Este PDF de 10 páginas está estructurado como un curso compacto:
- Portada
- Prefacio
- Índice
- 2 capítulos principales
- 2 anexos (ecuaciones y glosario)
Conceptos fundamentales desarrollados en el cuaderno
La energía libre de los electrones como fuerza motriz
- ΔG°’ = −nFΔE°’ como relación fundamental
- NADH → O₂ libera ~−220 kJ·mol⁻¹
- El Complejo I captura la primera etapa de ~−70 kJ·mol⁻¹
- El bombeo de protones es un trabajo termodinámicamente “ascendente”
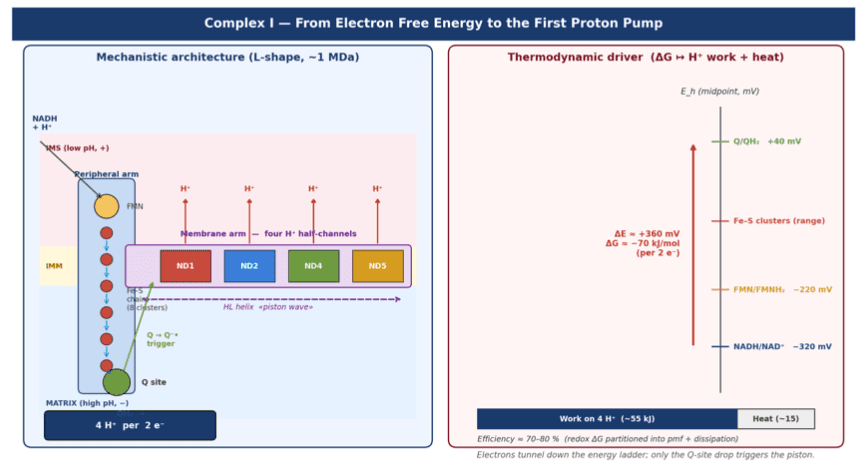
Mecanismo molecular — un pistón impulsado por redox
- Estructura en L (~1 MDa, 45 subunidades)
- Brazo redox: FMN + centros Fe–S (N1a → N2)
- Brazo de membrana: canales de protones ND1, ND2, ND4, ND5
- Semiquinona (Q⁻•) como desencadenante mecánico
- Hélice HL como transductor conformacional (~60 Å)
Ruta de transferencia electrónica:
NADH → FMN → centros Fe–S → Q → QH₂
El flujo de electrones no transporta protones directamente, sino que activa una onda conformacional que impulsa su translocación mediante canales de acceso alternante.
Estequiometría y comportamiento del sistema
- 1 NADH → 2 e⁻ → 4 H⁺ bombeados por el Complejo I
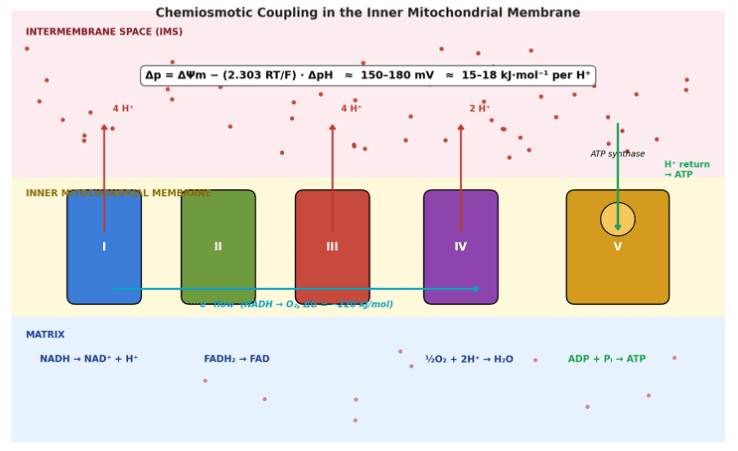
- Rendimiento total de la cadena respiratoria: 10 H⁺ por NADH
- Transporte inverso de electrones (RET) con Δp alto
- Principal fuente de ROS en estados hiperpolarizados
- Transición A↔D en isquemia
Marco cuantitativo y termodinámico
- ΔE (NADH → Q) ≈ +0.36 V
- ΔG ≈ −70 kJ·mol⁻¹
- Δp ≈ 180–220 mV
- Trabajo requerido: ~+77 kJ·mol⁻¹ para 4 H⁺
- Eficiencia ≈ 70–80 %
Relaciones clave:
- ΔG°’ = −nFΔE°’
- Δp = ΔΨ_m − (2.303 RT/F)·ΔpH
El Complejo I opera cerca del equilibrio, pero disipa parte de la energía para mantener el flujo direccional, en cumplimiento de la segunda ley de la termodinámica.
Relevancia clínica y traslacional
- Deficiencias del Complejo I (Leigh, MELAS, LHON)
- Lesión por isquemia-reperfusión y ROS por RET
- Metformina como inhibidor reversible
- Patologías por hiperpolarización vs despolarización
- Papel central en la disfunción mitocondrial
Ideas clave
- “El primer protón se paga con ~70 kJ·mol⁻¹ de energía electrónica”
- La semiquinona (Q⁻•) es un disparador mecánico, no un almacén de energía
- La hélice HL es un transductor mecánico de largo alcance
- Eficiencia < 100 % = producción necesaria de entropía
¿A quién va dirigido?
- Estudiantes de doctorado en bioenergética y biología molecular
- Médicos interesados en la fisiología mitocondrial
- Investigadores en biología redox
- Clínicos que estudian la disfunción mitocondrial
Idea clave
El Complejo I es un motor mecánico impulsado por reacciones redox que convierte la energía libre de los electrones en bombeo de protones, iniciando la fuerza protón-motriz y la producción de energía celular.
Nota: El PDF completo está en inglés.