Sobre este cuaderno
El potencial de membrana mitocondrial (ΔΨm) no es un valor estático, sino un equilibrio dinámico entre el bombeo de protones por la cadena de transporte de electrones y múltiples vías de disipación, incluyendo la síntesis de ATP, el transporte iónico y las fugas.
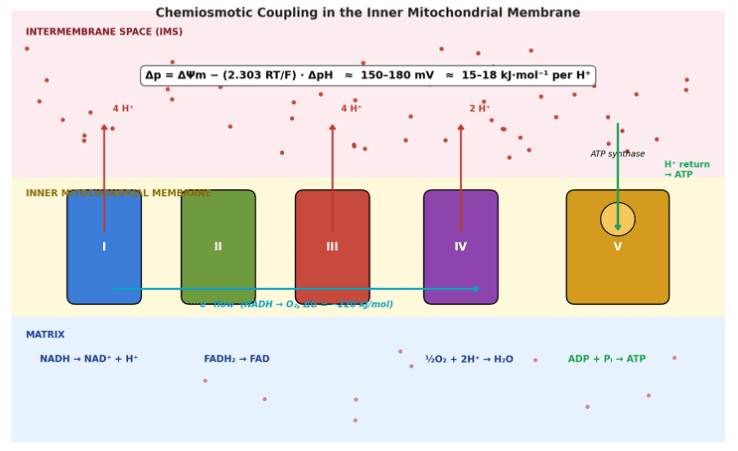
En condiciones fisiológicas, el ΔΨm se mantiene alrededor de 150–180 mV, contribuyendo a una fuerza protón-motriz total (Δp) de aproximadamente 180–220 mV. Este gradiente electroquímico captura una gran parte de los ~−220 kJ·mol⁻¹ liberados por la oxidación del NADH y alimenta la síntesis de ATP, el metabolismo y la señalización.
Este cuaderno de 15 páginas proporciona un marco estructurado y clínicamente aplicable para comprender la disfunción mitocondrial como una bifurcación entre dos estados opuestos:
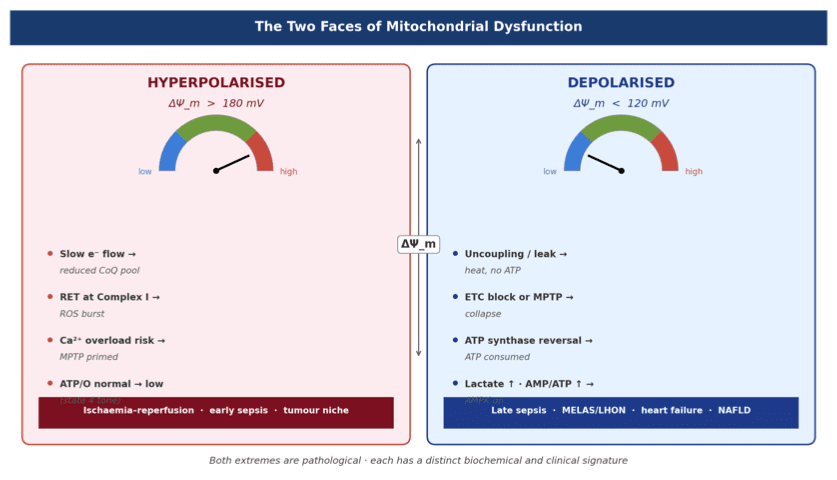
- Hiperpolarización (ΔΨm > 180 mV) : estado de alta energía, inestable, dominado por ROS
- Despolarización (ΔΨm < 120 mV) : fallo energético, déficit de ATP, colapso
Comprender esta distinción es esencial, ya que cada estado requiere estrategias terapéuticas opuestas.
Contenido del cuaderno (4 capítulos)
Capítulo 1 — Qué crea y aumenta el ΔΨm
Cinco palancas, por orden de peso cuantitativo :
- Bombeo vectorial de H⁺ por los complejos I (4 H⁺), III (4 H⁺), IV (2 H⁺) por 2 e⁻ = 10 H⁺/NADH
- Suministro de sustratos — ciclo de Krebs, β-oxidación, glutaminólisis, cuerpos cetónicos, lanzaderas malato-aspartato / glicerol-3-fosfato
- Disminución de la disipación — bajo ADP / Pi, inhibición de ANT o F₀ → respiración en estado 4 → hiperpolarización fisiológica
- Reducción de fugas — regulación de UCP, integridad de cardiolipina, crestas mitocondriales compactas (MICOS/OPA1), ensamblaje en supercomplejos
- Ajuste catión/H⁺ — cierre de K_ATP, equilibrio Na⁺/H⁺, Ca²⁺ matricial activando PDH y deshidrogenasas
Techo termodinámico: Δp máximo ≈ 200–230 mV.
Las mitocondrias sanas se sitúan alrededor de ~180 mV debido al aumento de fugas a valores más altos.
Contextos clínicos hiperpolarizados: isquemia-reperfusión, células tumorales, sepsis temprana, activación de linfocitos T.
Capítulo 2 — Qué disminuye el ΔΨm
Cinco categorías :
- A. Inhibición de la cadena de transporte de electrones (ETC) – rotenona / MPP⁺ / LHON (I), 3-NP / SDHx (II), antimicina A (III), CO / CN / NO (sepsis) (IV), pérdida de citocromo c
- B. Déficit de sustratos / cofactores – hipoxia, bloqueo del ciclo de Krebs, fallos en β-oxidación (CPT-II, MCAD, VLCAD), déficit de CoQ₁₀, defectos en clusters Fe–S (Friedreich)
- C. Aumento de fugas – DNP / FCCP, UCP1-3, ciclo de ácidos grasos, fuga vía ANT, peroxidación de cardiolipina
- D. Apertura del MPTP – sobrecarga de Ca²⁺ + estrés oxidativo, sensible a ciclosporina A, colapso catastrófico
- E. Inversión de la ATP sintasa – regulada por IF₁; consume ATP glucolítico para mantener ΔΨm residual
Bucle de despolarización autoamplificado : ΔΨm ↓ → mitofagia PINK1/Parkin → liberación de Ca²⁺ → activación AMPK → aumento de ROS → liberación de citocromo c → mayor pérdida de ΔΨm
Contextos clínicos despolarizados : sepsis tardía, insuficiencia cardíaca, neurodegeneración, MELAS / LHON / Leigh, fármacos mitotóxicos, NAFLD / NASH
Consecuencias inmunometabólicas : macrófagos bloqueados en M1/HIF-1α, fallo en transición de linfocitos T, inmunoparálisis
Jerarquía terapéutica : eliminar la agresión → restaurar sustratos/cofactores → equilibrar redox → estimular mitofagia → terapias experimentales
Capítulo 3 — Distinción clínica hiper vs hipo ΔΨm
Huella bioquímica (10 ejes) : flujo ETC, NADH/NAD⁺, redox CoQ, ROS, ATP/ADP, lactato, Ca²⁺, PINK1/Parkin, morfología, calor
Evaluación en 4 pasos :
- Valores clínicos basales: lactato, relación L/P (>25 → Bloqueo del complejo I/ETC), β-OHB/AcAc, acilcarnitinas.
- Funcional: OCR Seahorse, imágenes JC-1/TMRM, enzimología de biopsia muscular.
- Genotipo: secuenciación de ADNmt con heteroplasmia, panel nuclear, espectroscopia de RMN con pico de lactato.
- Huella dactilar direccional: síntesis a pie de cama.
Regla práctica :
- Alto nivel de ROS + ATP normal + contexto de reperfusión → disfunción hiperpolarizada.
- Alto nivel de lactato + bajo nivel de ATP + AMPK activada + marcadores de mitofagia + enfermedad crónica → disfunción despolarizada.
Direccionalidad terapéutica : antioxidantes ayudan en hiperpolarización pero empeoran despolarización; reposición metabólica rescata despolarización; mitocanes selectivos en tumores hiperpolarizados.
Capítulo 4 — Síntesis integradora
- Mapa del espacio de fases del triángulo ΔΨm × ROS × redox de los estados bioenergéticos.
- Árbol de decisiones a pie de cama (5 preguntas).
- Anclajes cuantitativos fáciles de memorizar: ΔΨm en reposo 150–180 mV, Δp 180–220 mV, 2,303RT/F ≈ 61,5 mV/pH, estequiometrías, anclajes ΔG, umbrales patológicos.
Anexos
- A. Ecuaciones clave : Δp, ΔG° = −nFΔE°, ΔG_phos, acumulación de Nernst, relación P/O. Constantes físicas.
- B. Glosario (16 términos) : ΔΨm, Δp, ETC, RET, MPTP, ANT, MCU, UCP, PINK1/Parkin, cardiolipina, JC-1/TMRM, relación L/P, β-OHB/AcAc, estados 3/4, mitocano, IF₁.
¿A quién va dirigido?
- Estudiantes de doctorado en bioenergética y fisiología
- Médicos y clínicos
- Investigadores en metabolismo e inmunología
- Profesionales interesados en la medicina mitocondrial
Idea clave
El ΔΨm no es simplemente “alto o bajo”, sino que define dos regímenes patológicos opuestos, cada uno requiriendo estrategias terapéuticas completamente diferentes.
Nota: El PDF completo está en inglés.