À propos de ce livret
Le potentiel de membrane mitochondriale (ΔΨm) n’est pas une valeur statique, mais un équilibre dynamique entre le pompage de protons par la chaîne de transport d’électrons et plusieurs voies de dissipation, incluant la synthèse d’ATP, le transport ionique et les fuites.
En conditions physiologiques, le ΔΨm est maintenu autour de 150–180 mV, contribuant à une force proton-motrice totale (Δp) d’environ 180–220 mV. Ce gradient électrochimique capture une grande partie des ~−220 kJ·mol⁻¹ libérés par l’oxydation du NADH et alimente la synthèse d’ATP, le métabolisme et la signalisation.
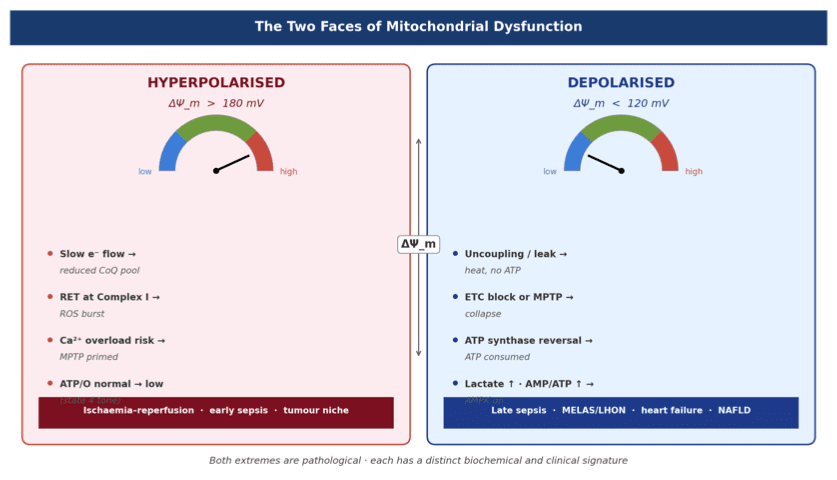
Ce livret de 15 pages propose un cadre structuré et cliniquement exploitable pour comprendre le dysfonctionnement mitochondrial comme une bifurcation entre deux états opposés :
- Hyperpolarisation (ΔΨm > 180 mV) : état à forte énergie, instable, dominé par les ROS
- Dépolarisation (ΔΨm < 120 mV) : défaillance énergétique, déficit en ATP, effondrement
Comprendre cette distinction est essentiel, car chaque état requiert des stratégies thérapeutiques opposées.
Contenu du livret (4 chapitres)
Chapitre 1 — Ce qui crée et augmente le ΔΨm
Cinq leviers, par ordre d’importance quantitative :
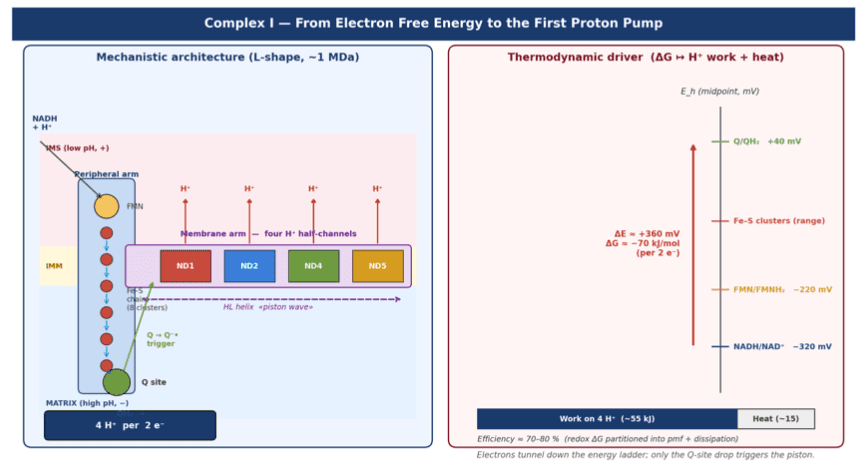
- Pompage vectoriel de H⁺ par les complexes I (4 H⁺), III (4 H⁺), IV (2 H⁺) par 2 e⁻ = 10 H⁺/NADH
- Apport en substrats — cycle de Krebs, β-oxydation, glutaminolyse, corps cétoniques, navettes malate-aspartate / glycérol-3-phosphate
- Diminution de la dissipation — faible ADP / Pi, inhibition de l’ANT ou du F₀ → respiration d’état 4 → hyperpolarisation physiologique
- Réduction des fuites — régulation des UCP, intégrité de la cardiolipine, crêtes mitochondriales compactes (MICOS/OPA1), assemblage en supercomplexes
- Ajustement cation/H⁺ — fermeture des canaux K_ATP, équilibre Na⁺/H⁺, Ca²⁺ matriciel physiologique activant la PDH et trois déshydrogénases
Plafond thermodynamique : ΔG_phos ≈ −56 à −60 kJ·mol⁻¹ et n ≈ 2,7 H⁺/ATP → Δp maximal ≈ 200–230 mV.
Les mitochondries saines se stabilisent autour d’un « plafond souple » d’environ 180 mV, car les fuites deviennent non ohmiques au-delà.
Contextes cliniques hyperpolarisés : ischémie–reperfusion (burst de ROS via RET), cellules tumorales (ΔΨm supranormal, sensibles aux mitocans), sepsis précoce, activation des lymphocytes T effecteurs.
Chapitre 2 — Ce qui diminue le ΔΨm
Cinq catégories :
- A. Inhibition de la chaîne de transport d’électrons (ETC) – rotenone / MPP⁺ / LHON (I), 3-NP / SDHx (II), antimycine A (III), CO / CN / NO (sepsis) (IV), perte du cytochrome
- B. Déficit en substrats / cofacteurs – hypoxie, blocage du cycle de Krebs, défaillances de la β-oxydation (CPT-II, MCAD, VLCAD), déficit en CoQ₁₀, anomalies des clusters Fe–S (ataxie de Friedreich)
- C. Augmentation des fuites – DNP / FCCP, UCP1-3, cycle des acides gras, fuite via ANT, peroxydation de la cardiolipine
- D. Ouverture du MPTP – surcharge en Ca²⁺ + stress oxydatif, sensible à la cyclosporine A, effondrement catastrophique
- E. Inversion de l’ATP synthase – régulée par IF₁ ; consomme l’ATP glycolytique pour maintenir un ΔΨm résiduel
Boucle de dépolarisation auto-amplifiée : ΔΨm ↓ → mitophagie PINK1/Parkin → libération de Ca²⁺ → activation AMPK → burst de ROS → libération du cytochrome c → perte accrue de ΔΨm
Contextes cliniques dépolarisés : sepsis tardif (hypoxie cytopathique), insuffisance cardiaque, neurodégénérescence, MELAS / LHON / Leigh, médicaments mitotoxiques (metformine, NRTI, linézolide, valproate), NAFLD / NASH
Conséquences immunométaboliques : verrouillage des macrophages en phénotype M1/HIF-1α ; échec de transition des lymphocytes T effecteurs vers mémoire ; immunoparalysie du sepsis
Hiérarchie thérapeutique (5 niveaux) : supprimer l’agression → restaurer substrats/cofacteurs → tamponner le redox → stimuler la mitophagie → approches expérimentales (élamipretide, restauration du NAD⁺, thérapie génique)
Chapitre 3 — Distinction clinique hyper- vs hypo-ΔΨm
Empreinte biochimique (10 axes) : flux ETC, NADH/NAD⁺, redox CoQ, ROS, ATP/ADP, lactate, gestion du Ca²⁺, PINK1/Parkin, morphologie, production de chaleur
Bilan en quatre étapes :
- Clinique de base — lactate, ratio L/P (>25 → blocage Complexe I / ETC), β-OHB / AcAc, acylcarnitines
- Fonctionnel — OCR Seahorse, imagerie JC-1 / TMRM, enzymologie sur biopsie musculaire
- Génétique — séquençage mtDNA (hétéroplasmie), panel nucléaire, spectroscopie RMN (pic lactate)
- Empreinte directionnelle — synthèse clinique au lit du patient
Règle pratique :
- ROS élevés + ATP normal + contexte de reperfusion → dysfonction hyperpolarisée
- Lactate élevé + ATP bas + AMPK activée + marqueurs de mitophagie + maladie chronique → dysfonction dépolarisée
Orientation thérapeutique (insight clé) : les antioxydants et découplants légers protègent en hyperpolarisation mais aggravent la dépolarisation ; la restauration des substrats/cofacteurs et l’activation de la mitophagie corrigent la dépolarisation mais pas l’hyperpolarisation ; les mitocans lipophiles cationiques sont sélectivement cytotoxiques pour les mitochondries tumorales hyperpolarisées (loi d’accumulation exp(FΔΨm/RT)).
Chapitre 4 — Synthèse intégrative
- Carte de phase ΔΨm × ROS × redox des états bioénergétiques
- Arbre décisionnel clinique (5 questions)
- Repères quantitatifs mémorisables : ΔΨm au repos 150–180 mV, Δp 180–220 mV, 2.303RT/F ≈ 61,5 mV/pH, stœchiométries, ΔG, seuils pathologiques
Annexes
- A. Équations clés : Δp, ΔG° = −nFΔE°, ΔG_phos, accumulation selon Nernst, ratio P/O. Constantes physiques.
- B. Glossaire (16 entrées) : ΔΨm, Δp, ETC, RET, MPTP, ANT, MCU, UCP, PINK1/Parkin, cardiolipine, JC-1/TMRM, ratio L/P, β-OHB/AcAc, états 3/4, mitocan, IF₁.
À qui s’adresse ce contenu ?
- Doctorants en bioénergétique et physiologie
- Médecins et cliniciens
- Chercheurs en métabolisme et immunologie
- Professionnels intéressés par la médecine mitochondriale
Aperçu clé
Le ΔΨm ne se résume pas à « élevé ou faible » — il définit deux régimes pathologiques opposés, chacun nécessitant des stratégies thérapeutiques fondamentalement différentes.
Note : Le PDF complet est en anglais.