À propos de ce livret
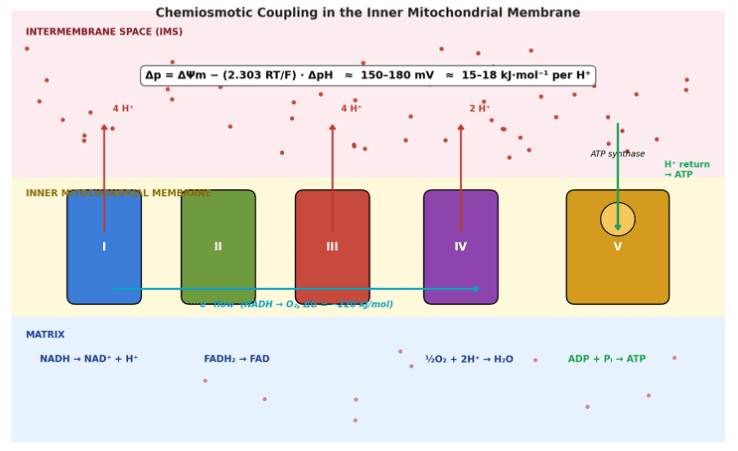
La force proton-motrice (Δp = ΔΨ_m − (2,303 RT/F)·ΔpH) constitue la monnaie énergétique centrale du vivant. Générée par la chaîne de transport d’électrons, elle capte une grande partie de l’énergie libre libérée par l’oxydation du NADH et la redistribue entre la synthèse d’ATP, les processus de transport et les voies de signalisation.
En conditions physiologiques (ΔΨ_m ≈ −150 à −180 mV, ΔpH ≈ 0,5–1), les mitochondries convertissent l’énergie redox en un gradient électrochimique d’environ 180–220 mV, correspondant à ~17–21 kJ/mol par proton.
Ce livret de 13 pages, rédigé en avril 2026, propose un cadre à la fois compact et rigoureux pour comprendre comment Δp est générée, quantifiée et altérée dans les maladies. Il relie les principes thermodynamiques aux systèmes biologiques réels, avec des dérivations numériques explicites et des implications cliniques.
Contenu du livret (5 modules)
Module 1 — Qu’est-ce que la force proton-motrice ?
- Mitchell (1961) : le produit immédiat de la respiration n’est pas un intermédiaire chimique mais un champ électrochimique à travers la membrane interne mitochondriale
- Δp comporte deux composantes additives : électrique (ΔΨ_m) + chimique équivalente en tension (ΔpH)
- Δp physiologique ≈ 180–220 mV → ~19–21 kJ/mol par proton
Module 2 — La composante électrique (ΔΨ_m)
- La chaîne respiratoire agit comme une pompe vectorielle de charges. La matrice perd des charges positives → devient électronégative (−150 à −180 mV)
- Stœchiométrie : Complexe I = 4 H⁺, III = 4 H⁺, IV = 2 H⁺ par 2 e⁻ (Complexe II = 0)
- Environ 75–80 % de la force proton-motrice totale réside dans ΔΨ_m chez les mitochondries de mammifères
- Clinique : Sondes TMRM / JC-1 ; metformine (Complexe I), roténone, oligomycine, FCCP ; une dépolarisation persistante prédit la mortalité dans le sepsis
Module 3 — La composante chimique (ΔpH)
- La matrice est plus alcaline de 0,5 à 1 unité de pH en raison de l’éjection des protons et du pouvoir tampon (phosphate, carboxylates, histidines)
- ΔΨ_m et ΔpH sont thermodynamiquement interconvertibles : valinomycine → dissipe ΔΨ_m, nigéricine → dissipe ΔpH, FCCP / CCCP / DNP → dissipent les deux
- Expérience du bain acide de Jagendorf (1966, chloroplastes) : la synthèse d’ATP peut fonctionner uniquement à partir du ΔpH
Module 4 — Quantification de la force proton-motrice (facteur de Nernst)
- Dérivation complète : de Δμ̃_H⁺ = F·ΔΨ_m − 2,303 RT·ΔpH vers la forme en tension : Δp = ΔΨ_m − (2,303 RT/F)·ΔpH
- À 37 °C : 2,303 RT/F ≈ 61,5 mV par unité de pH.
- Exemple de calcul : ΔΨ_m = −170 mV, ΔpH = 0,6 → Δp ≈ 207 mV → ~20 kJ/mol H⁺ → 10 H⁺ × 20 = ~200 kJ/mol capturés par NADH → ~91 % des ~220 kJ/mol libérés par NADH → O₂. À une PMF plus faible (155–180 mV), la fraction capturée chute dans la plage 150–175 kJ/mol (68–80 %) décrite dans les manuels.
- Plafond de synthèse de l’ATP : ΔG_ATP ≤ ~4 H⁺ × 20 kJ = ~80 kJ/mol ATP; Valeur mesurée : ~55–60 kJ/mol (~70 % du maximum théorique). L’écart correspond à la dissipation nécessaire au maintien du flux imposé par la seconde loi de la thermodynamique.
Module 5 — Intégration, physiologie et pertinence clinique
- La force proton-motrice (Δp) contrôle : l’entrée mitochondriale de Ca²⁺ via MCU, la production de ROS (via transport inverse d’électrons au Complexe I), la signalisation de la mitophagie PINK1/Parkin, l’import protéique via TIM23
- Découplage contrôlé : Les UCP1–3 et les découplants thérapeutiques (ex : BAM15) dissipent Δp sous forme de chaleur — ce n’est pas un défaut mais une fonction physiologique.
- Phénotypes immunométaboliques : Lymphocytes T effecteurs / macrophages M1 → Δp bas, glycolyse dominante (type Warburg), Lymphocytes mémoire / T régulateurs → ΔΨm élevé, OXPHOS + β-oxydation, Cellules sénescentes → Δp bas et instable
- Cascade d’effondrement de la PMF : Atteinte de la chaîne respiratoire → dépolarisation → inversion de l’ATP synthase → ouverture du MPTP → libération du cytochrome c → inflammation stérile induite par DAMP (cGAS-STING, TLR9)
- Axes thérapeutiques : Précurseurs du NAD⁺ (NMN, NR); Stabilisation de la cardiolipine (SS-31 / élamipretide); Médicaments ciblant la mitochondrie (MitoQ, MitoTEMPO); Transplantation mitochondriale
Équations clés
- PMF (Mitchell) : Δp = ΔΨ_m − (2,303 RT/F)·ΔpH
- Énergie par proton : ΔG = F·Δp ≈ 17–21 kJ/mol
- Énergie capturée par NADH : 10 H⁺ × F·Δp ≈ 150–200 kJ/mol
- Variation redox NADH → O₂ : ΔG°’ = −nFΔE°’ ≈ −220 kJ/mol
- Facteur de Nernst (37 °C) : 61,5 mV/pH
- Plafond ATP : ΔG_ATP ≤ ~80 kJ/mol (mesuré : −55 à −60 kJ/mol)
À qui s’adresse ce contenu ?
- Doctorants en sciences du vivant, biophysique et bioénergétique
- Médecins souhaitant une compréhension quantitative de la fonction mitochondriale
- Chercheurs en biologie redox et métabolisme systémique
- Cliniciens explorant l’immunométabolisme et la médecine mitochondriale
Aperçu clé
La force proton-motrice est la batterie électrochimique universelle du vivant : elle est générée par la respiration, consommée par le travail cellulaire, et son effondrement constitue une signature quantitative de la maladie.
Note : Le PDF complet est en anglais.