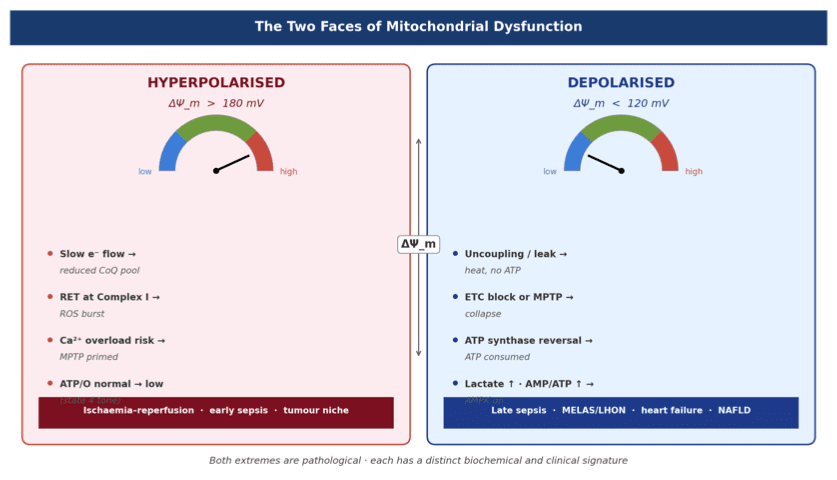
El principio biológico fundamental
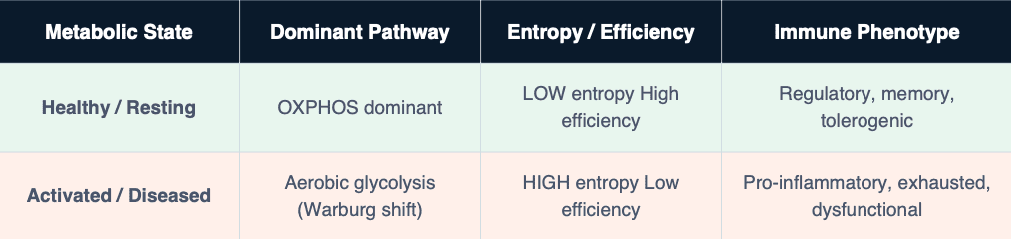
Cada macrófago toma una decisión termodinámica. Puede funcionar mediante fosforilación oxidativa (OXPHOS), un estado metabólico de alta eficiencia y baja entropía, o bien optar por la glucólisis aeróbica, un modo rápido, ineficiente y de alta entropía. Este eje termodinámico determina si la célula inmunitaria cura o daña al huésped.
Este compromiso bioenergético no es un efecto secundario de la enfermedad. Es el motor molecular de la enfermedad. La misma lógica se reproduce de forma idéntica en tres condiciones clínicamente distintas: la sepsis, la artritis reumatoide y el cáncer de pulmón.
Comparación de los fenotipos bioenergéticos
1. Sepsis — Cuando el motor se sobrecalienta
En la sepsis, las señales bacterianas colapsan el potencial de membrana mitocondrial (∆Ψm), inundan la célula con especies reactivas de oxígeno (ROS) y fuerzan un cambio metabólico de OXPHOS a glucólisis. El resultado es la hiperpolarización de los macrófagos M1: liberación masiva de IL-1β, TNF-α e IL-6 — la tormenta de citocinas. Esto no es solo inflamación; es un fallo termodinámico. La célula disipa energía en forma de calor y entropía en lugar de generar trabajo biológico útil.
Mecanismos moleculares
• Explosión de ROS desde los complejos I/III → estabilización de HIF-1α → aumento de la expresión de genes glucolíticos
• Pérdida de ∆Ψm → acoplamiento defectuoso de la ATP sintasa → fuga de protones en forma de calor
• Liberación de mtDNA al citosol → activación de cGAS-STING → amplificación de la respuesta inmunitaria innata
• Acumulación de succinato → estabilización postraduccional de HIF-1α e IL-1β
✓ Traducción clínica
• Precursores de NAD+ (NMN, NR): restauran la disponibilidad de cofactores del complejo I, recuperan la capacidad OXPHOS y reducen la producción de citocinas M1 en modelos preclínicos de sepsis.
• Antioxidantes dirigidos a la mitocondria (MitoQ, SS-31): eliminan el superóxido generado en la membrana mitocondrial interna (IMM), preservan ∆Ψm y atenúan el daño orgánico en modelos CLP.
• Oportunidad de biomarcador: relación OCR/ECAR (consumo de oxígeno vs acidificación extracelular) como índice metabólico del estado inflamatorio de los macrófagos.
2. Artritis reumatoide — La entropía como estado crónico
La articulación sinovial en la artritis reumatoide es un microentorno permanentemente de alta entropía: hipóxico, pobre en glucosa, ácido y saturado de lactato. Las células T CD4+, los macrófagos y los sinoviocitos tipo fibroblasto convergen hacia la glucólisis aeróbica para sobrevivir. Este cambio metabólico es la inflamación misma — mantiene HIF-1α, activa NF-κB y sostiene el inflamasoma NLRP3. Mientras tanto, las células T reguladoras (Treg), que dependen de la oxidación de ácidos grasos y del OXPHOS para su función supresora, están metabólicamente privadas en este mismo entorno.
Mecanismos moleculares
• HIF-1α → aumento de GLUT1/LDHA → incremento del flujo glucolítico → producción de IL-17 e IL-6
• ROS mitocondriales → activación de NF-κB y NLRP3 → bucle inflamatorio sostenido
• Activación de mTORC1 → supresión de OXPHOS → desviación de células T de Treg hacia Th17
• Treg dependientes de FAO: privación de sustratos energéticos (baja disponibilidad lipídica en articulaciones hipóxicas) = pérdida de regulación inmunitaria
✓ Traducción clínica
• Metformina: inhibidor del complejo I → activa AMPK, restaura el equilibrio metabólico y reduce el flujo glucolítico en células inmunitarias de la AR. Efecto antiinflamatorio independiente de su acción hipoglucemiante.
• Inhibidores de mTOR (análogos de rapamicina): cambian el destino de las células T de Th17 hacia Treg al reactivar OXPHOS y FAO.
• Oportunidad de biomarcador: relación P/O (ATP producido por O₂ consumido) y relación NAD+/NADH en células inmunitarias sinoviales como métricas cuantitativas de la actividad de la enfermedad.
3. Cáncer de pulmón — El tumor como una trampa termodinámica
Los tumores pulmonares exportan entropía a su microentorno. Consumen glucosa de forma agresiva mediante el efecto Warburg, liberan lactato que acidifica el medio y agotan el O₂ — creando una prisión termodinámica para los linfocitos infiltrantes del tumor (TILs). Los TILs presentan una disminución en la tasa de consumo de oxígeno, una reducción de la masa mitocondrial y un colapso del ∆Ψm. El agotamiento de las células T no es solo un programa transcripcional — es un colapso bioenergético. El tumor no solo se oculta del sistema inmunitario: lo priva de recursos.
Mecanismos moleculares
• Glucólisis tipo Warburg en células tumorales → liberación de lactato → acidificación del microentorno tumoral (TME) → inhibición de OXPHOS en células T
• Depleción de glucosa/glutamina en el TME → TILs privados de sustratos → pérdida de ∆G efectivo
• Hipoxia → HIF-1α en el tumor → aumento de VEGF/PD-L1 → exclusión inmunitaria y agotamiento de checkpoints
• Fenotipo TIL CD36 alto: exceso de captación lipídica → sobrecarga lipídica mitocondrial → susceptibilidad a la ferroptosis
✓ Traducción clínica
• Combinación metabólica + checkpoint: potenciadores de OXPHOS (urolitina A, NMN) combinados con anti-PD-1 muestran una reactivación sinérgica de los TILs en modelos preclínicos de NSCLC.
• Intervención nutricional: la restricción de metionina reduce la supresión de Treg; la suplementación con glutamina restaura la capacidad respiratoria de los TILs.
• Oportunidad de biomarcador: perfilado OCR de TILs (tecnología Seahorse) antes del tratamiento; resonancia magnética con piruvato 13C hiperpolarizado para el mapeo metabólico en tiempo real del TME.
Perspectiva termodinámica y cuantitativa
Cada enfermedad representa una desviación medible de la eficiencia termodinámica. Las variables clave no son solo moleculares — son parámetros bioenergéticos cuantificables que pueden monitorizarse clínicamente:
• ∆Ψm (potencial de membrana mitocondrial): índice de la fuerza protón-motriz y del acoplamiento de OXPHOS. Su colapso precede a la disfunción inmunitaria.
• Relación P/O (eficiencia de fosforilación): ATP producido por molécula de O₂ consumida. Disminuye con la reprogramación inflamatoria.
• Relación OCR/ECAR: consumo de oxígeno vs tasa de acidificación extracelular — índice en tiempo real del equilibrio OXPHOS/glucólisis.
• Relación NAD+/NADH: sensor redox maestro. Un NAD+ bajo = OXPHOS alterado, mayor entropía y regulación inmunitaria dependiente de sirtuinas comprometida.
• Número de copias de mtDNA / mtDNA citosólico: indicador de acumulación de entropía mitocondrial y de activación innata mediada por DAMPs.
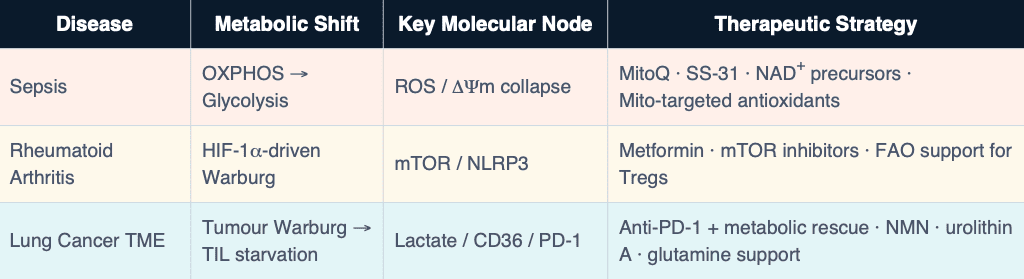
Marco clínico unificado
Hacia dónde se dirige: biomarcadores inmunitarios de nueva generación
La próxima generación de biomarcadores inmunitarios no se limitará a las citocinas. Será metabólica:
• Relación OCR/ECAR en células inmunitarias de sangre periférica
• Potencial de membrana mitocondrial (∆Ψm) como índice de activación inmunitaria
• Relación NAD+/NADH como indicador sistémico de salud bioenergética
• Tasa de liberación de mtDNA como marcador en tiempo real de producción de entropía
• Relación lactato/piruvato urinaria como indicador no invasivo del cambio hacia la glucólisis
Las terapias futuras no se limitarán a bloquear receptores — restaurarán el orden termodinámico en las células inmunitarias que lo han perdido. Esta es la promesa de la inmunometabolismo: no más inmunosupresores, sino estrategias bioenergéticas más inteligentes que devuelvan a las células inmunitarias lo que la enfermedad les ha quitado.
Base de evidencia seleccionada
1. Ji F et al. Crosstalk of mitochondrial dysfunction and macrophage polarization in sepsis. Front Immunol. 2026.
2. Xie R et al. Roles of immune cell metabolism in rheumatoid arthritis. Front Immunol. 2026.
3. Eivazzadeh Y et al. Immunometabolism in lung cancer. iScience. 2026.
4. Dwivedi V et al. Mitochondrial dysfunction and cellular senescence in ageing sarcopenia. Mol Biol Rep. 2026.
5. Seledtsov V. Mitochondria-targeted therapy in anti-aging medicine. J Biol Methods. 2026.
6. Glogowski PA et al. Reprogramming the mitochondrion in atherosclerosis. Antioxidants. 2025.
7. Xu Y et al. Nutritional intervention alleviates T cell exhaustion and empowers anti-tumor immunity. Front Immunol. 2026.
8. Zhang XY et al. The role of CD36 in immune function. Front Immunol. 2026.
Este documento es una comunicación científica basada en evidencia, destinada a profesionales de la salud, investigadores y estudiantes avanzados. Todas las afirmaciones se basan en literatura revisada por pares hasta el primer trimestre de 2026. No está destinado como guía clínica directa.